Vacinação contra COVID começa no dia 27 de fevereiro seguindo grupos prioritários
Leia também:
As vacinas bivalentes contra a COVID integram a segunda geração de imunizantes contra a doença. E saiba que atualizar vacinas é algo natural. Basta pensar na gripe, infecção aguda do sistema respiratório, provocado pelo vírus da influenza, com grande potencial de transmissão, com quatro tipos de vírus influenza: A, B, C e D. O vírus influenza A e B são responsáveis por epidemias sazonais, sendo o vírus influenza A responsável pelas grandes pandemias. POr isso, todo ano tem campanha de vacinação contra a gripe.
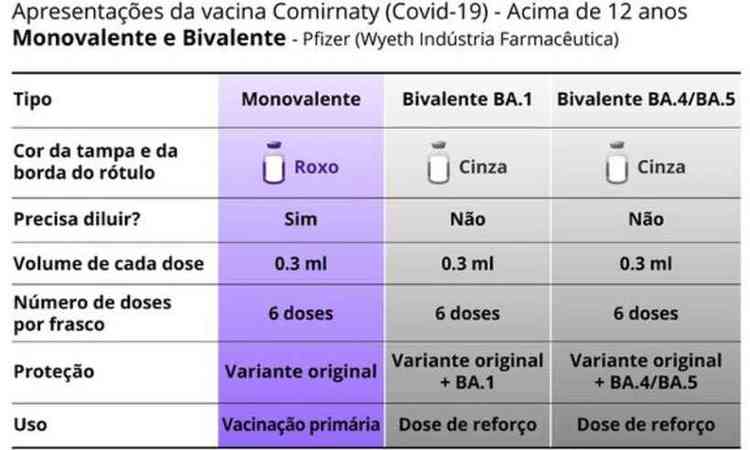
ilustração de quadro das vacinas bivalente e monovalente
Anvisa/Repdodução- Identificadas por tampa na cor cinza. O rótulo trará a seguinte identificação: Comirnaty® Bivalente BA.1 ou Comirnaty® Bivalente BA.4/BA.5.
- Cada frasco possui seis doses e a vacina não deve ser diluída.
- Indicadas para a população a partir de 12 anos.
- Indicadas como reforço. Devem ser aplicadas a partir de três meses após a série primária de vacina ou reforço anterior.
- Validade de 12 meses, quando estocadas de -80°C a -60°C ou de -90°C a -60°C.
- Podem ser armazenadas em geladeira, entre 2°C e 8°C, por um único período de até dez semanas, não excedendo a data de validade original.


*Para comentar, faça seu login ou assine