As reuniões públicas do colegiado da Anvisa costumam ser transmitidas ao vivo pelo canal da Agência no YouTube. Segundo o órgão, a reunião será às 10h e terá transmissão nos canais digitais da Anvisa e pela EBC.
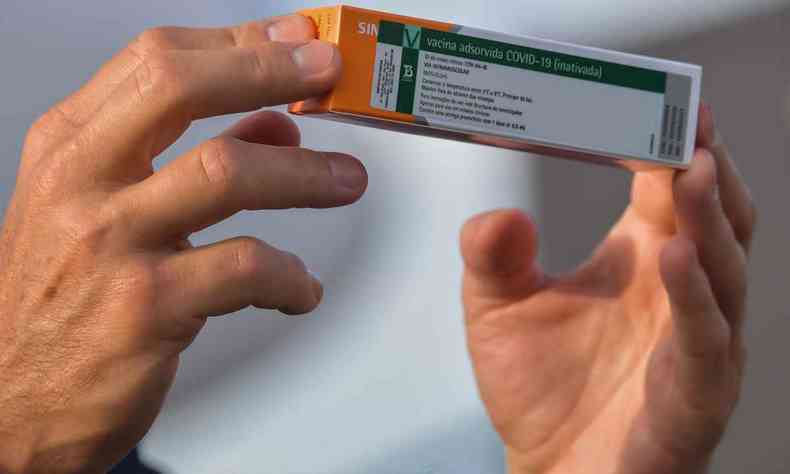
A Anvisa estipulou dez dias como tempo para analisar as solicitações emergenciais, feitas na sexta-feira (08/01). A reunião, portanto, ocorrerá dois dias antes do encerramento do prazo. O imunizante do Butantan é a CoronaVac, de origem chinesa. O composto da Fiocruz, por sua vez, foi desenvolvido pela Universidade de Oxford, no Reino Unido, em parceria com o laboratório AstraZeneca.
Ao confirmar a previsão de reunião para o domingo, a Anvisa explicou que a análise depende da entrega de documentos faltantes necessários para embasar os pedidos de uso emergencial.
Segundo informações fornecidas pela agência no início da tarde desta quarta (13/01), 40,7% da documentação necessária para o aval da vacina do Butantan já teve a análise concluída. Outros 24,07% ainda estão sendo verificados pelos técnicos da Anvisa, enquanto 29,76% necessitam de complementação. Há, ainda, 5,47% de documentos ainda não entregues.
No que tange à Fiocruz, 32,6% da documentação teve a análise concluída. Enquanto isso, 49,02% está em análise e 18,38% dos papéis necessitam de complementos. O governo federal espera o aval da Anvisa para iniciar o plano nacional de imunização para conter a pandemia.
Se ao menos uma autorização emergencial for dada já no domingo, o Palácio do Planalto poderá começar a vacinar os brasileiros em 20 de janeiro, data mais otimista projetada pelo ministro da Saúde, Eduardo Pazuello.
Passos para autorização
Durante a análise das documentações referentes aos imunizantes, a Anvisa solicita uma série de informações, como a descrição da vacina, o histórico do relacionamento entre a fabricante e agência reguladora e o andamento dos processos internacionais de liberação do composto em análise.
O médico e contra-almirante Antonio Barra Torres, indicado por Jair Bolsonaro (sem partido), é o presidente da Anvisa e um dos componentes do colegiado que definirá sobre o uso emergencial das vacinas.
Além de Fiocruz e Butantan, outras duas vacinas estão sendo analisadas pela Anvisa. Uma, é desenvolvida pela Pfizer; a outra, pela Janssen. As duas companhias, entretanto, não solicitaram a liberação emergencial.
Quem poderá ser vacinado?
A concessão de autorizações emergenciais não significa o início de uma campanha universal de vacinação. Nesse modelo de aval, os fabricantes são autorizados a aplicar a doses em grupos previamente definidos, com os profissionais de saúde. Em dezembro, Eduardo Pazuello chegou a dizer que os imunizados na fase emergencial precisarão assinar um termo de consentimento oficializando a concordância com a aplicação.
Doria quer vacina logo após aval da Anvisa
Nesta quarta, o governador paulista, João Doria (PSDB), um dos mais ferrenhos defensores da CoronaVac na classe política, demonstrou a intenção de iniciar a imunização em seu estado tão logo o aval da Anvisa seja dado. Originalmente, a ideia do tucano era começar a campanha no próximo dia 25.
“Todas as vacinas consideradas eficazes, de acordo com os cientistas que dão depoimentos e estudam o tema, são as que atendem 50% ou mais de eficácia. Portanto, a vacina do Butantan atende plenamente. E, atendendo plenamente, deve ser colocada imediatamente após a aprovação da Anvisa, para a vacinação dos brasileiros”, disse.
“Aproveito para dizer aqui e desejar, esperar, que a Anvisa cumpra seu dever científico e humanitário no próximo domingo, liberando as duas vacinas”, completou, mencionando também o material desenvolvido por Oxford/AstraZeneca.
As doses em jogo
O pedido de emergência da Fiocruz contempla 2 milhões de unidades da vacina, importadas da Índia. O Butantan, por seu turno, quer utilizar seis milhões de doses vindas da China. A SinoVac tem eficácia global próxima de 50%.
